
EU-Vertrag mit Pfizer: „Langfristige Wirkungen und Wirksamkeit des Impfstoffs derzeit nicht bekannt“
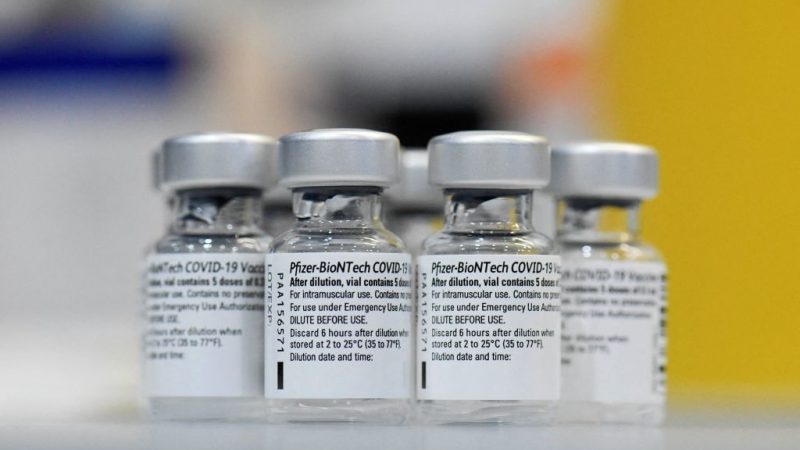
Bereits im März 2021 war die belgische Vereinigung „Notre Bon Droit“ in den Besitz einer geleakten Fassung des Impfstoff-Vertrages zwischen der EU und dem Pfizer-Konzern gelangt. Mittlerweile ist das Dokument in einer ungeschwärzten Fassung der Öffentlichkeit zugänglich. Es offenbart ähnliche Vertragsinhalte, wie sie bezüglich der Beschaffung des von BioNTech entwickelten Corona-Impfstoffs „Comirnaty“ in anderen Ländern vereinbart waren.
Kritik an Intransparenz der EU bezüglich der Beschaffung der Impfstoffe
Die Impfstoff-Verträge der EU waren schon bisher Gegenstand verbreiteten Argwohns. Kritik riefen unter anderem die Modalitäten ihres Zustandekommens hervor. Dazu gehörte die Löschung eines SMS-Verkehrs zwischen Kommissionspräsidentin Ursula von der Leyen und Pfizer-CEO Albert Bourla im Vorfeld einer Vertragsunterzeichnung.
Die Kommissionspräsidentin soll die Kompetenzen in Sachen Impfstoffbeschaffung an sich gezogen haben. Dies habe möglicherweise nicht nur mögliche Vereinbarungen zu günstigeren Preiskonditionen verhindert – und die Abhängigkeit von einem bestimmten Anbieter verstärkt. Vor allem habe von der Leyen über Transparenzbestimmungen der EU selbst hinweggesehen.
Die Veröffentlichung des ungeschwärzten Vertragstextes zwischen der EU und Pfizer zur Vorbestellung von Impfstoff (APA) vom 20. November 2020 bestätigt jedoch auch noch andere Vorahnungen.
EU musste 700 Millionen Euro als Anzahlung leisten
Was vielfach hinter vorgehaltener Hand und gerüchteweise kolportiert wurde, geht nun auch aus dem ungeschwärzten Text hervor. Demnach haben die EU und ihre Mitgliedstaaten ihre Exit-Strategie aus den Corona-Maßnahmen auf einen Impfstoff aufgebaut, zu dem zahlreiche Fragen offen waren.
Der Inhalt des Vertrages zwischen Pfizer und der EU folgt in entscheidenden Passagen dem, was bereits zuvor enthüllte Verträge mit anderen Staaten offenbarten. Zuvor war es NGOs in Südafrika und Brasilien gelungen, die Offenlegung der Vereinbarungen mit den Herstellern zu erzwingen.
Gegenüber Pfizer hatte sich die EU dazu verpflichtet, 15,50 Euro pro Dosis für vorerst 200 Millionen Dosen zu bezahlen. Dabei war für die ersten 100 Millionen ein Stückpreis von 17,50 und für die weiteren einer von 13,50 Euro vereinbart – ohne Mehrwertsteuer. Hätte die EU weniger geordert, wäre der Preis für die Dosis deutlich nach oben korrigiert worden.
Die EU musste 700 Millionen Euro im Voraus entrichten. Für den Fall eines Lieferverzuges hatte sie zwar mehr Rechte eingeräumt bekommen als beispielsweise Südafrika, dennoch hatte Pfizer sich einige weitreichende Haftungsbeschränkungen für den Fall von Engpässen ausbedungen.
Impfstoff „rasch entwickelt“ – mögliche „nachteilige Wirkungen“ nicht auszuschließen
Als noch pikanter erscheint vielen, dass die EU Pfizer als Hersteller von fast allen Schadensersatzpflichten im Zusammenhang mit möglichen Impfschäden im Voraus freigezeichnet hat. Diese Verpflichtung solle auch für die teilnehmenden Mitgliedstaaten gelten.
Im Annex I, der sich mit den Modalitäten der Bestellung befasst, heißt es, der teilnehmende Mitgliedstaat erkenne an, dass
der Impfstoff und die mit dem Impfstoff zusammenhängenden Materialien sowie ihre Komponenten und Bestandteile aufgrund der Notsituation der COVID-19-Pandemie rasch entwickelt werden und nach der Bereitstellung des Impfstoffs an die teilnehmenden Mitgliedstaaten im Rahmen des APA weiter untersucht werden.“
Zudem erkenne der Staat an, dass „die langfristigen Wirkungen und die Wirksamkeit des Impfstoffs derzeit nicht bekannt sind“. Die Wissenserklärung umfasst auch „nachteilige Wirkungen des Impfstoffs“, die es „geben kann“ und die „derzeit nicht bekannt sind“.
Staaten mussten ausreichende Mittel für mögliche Entschädigungen nachweisen
Mit der Bestellung sichert der teilnehmende Mitgliedstaat zu, dass alle für die Verwendung der Präparate erforderlichen Genehmigungen vor dem Zeitpunkt der Erfüllung vorliegen. Auch dies vermindert mögliche Haftungsansprüche gegen den Hersteller noch zusätzlich.
Im Kern mussten sich also die Mitgliedstaaten verpflichten, für den Fall des Auftretens von Impfschäden die Geschädigten aus eigenen Mitteln schadlos zu halten. Sie mussten zudem zusichern, dafür über angemessene gesetzliche oder regulatorische Befugnisse und angemessene Finanzmittel zu verfügen.
Die Kommission erklärte im Namen ihrer teilnehmenden Mitgliedstaaten, dass die Verwendung der Impfstoffe „unter epidemischen Bedingungen“ erfolge. Diese erforderten eine solche Verwendung, weshalb deren Verabreichung „unter der alleinigen Verantwortung der teilnehmenden Mitgliedstaaten erfolgt“.
Ersatzpflichten für Schäden sollten im Regelfall die Mitgliedstaaten selbst treffen
Ausnahmen waren lediglich für Fälle des vorsätzlichen Handelns oder einer Abweichung von den zugesicherten Spezifikationen vorgesehen. Der Hersteller sagte auch eine Produktion „in Übereinstimmung mit der aktuellen Guten Herstellungspraxis (GMP)“ zu.
Pfizer und BioNTech sagten auch den Abschluss von Versicherungen zu, wie sie bei pharmazeutischen Industrieunternehmen in ähnlicher Lage üblich seien. Diese beziehe sich jedoch auf Haftungen im Zusammenhang mit den Tätigkeiten im Rahmen der Erfüllung der Vereinbarung. Es wurde explizit noch einmal darauf hingewiesen, dass es sich weder um eine Produkthaftpflicht noch eine allgemeine Versicherung dieser Art handele.
Im Kern sollten die Mitgliedstaaten auch Folgen eines Rückrufs selbst tragen. Für einen solchen Fall oder den einer Nichtlieferung aufgrund eines vermuteten GMP-Verstoßes bestand jedoch die Option, ein Gutachten einzuholen. Dafür solle der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur (EMA) zuständig sein. Er solle klären, inwieweit der jeweilige Schritt gerechtfertigt gewesen sei.






![A100 in Berlin: So geht es nach der Stillegung der Ringbahnbrücke weiter [Pressekonferenz]](https://images-de.epochtimes.de/uploads/2025/03/Thumbnail-Autobahn-GmbH-Update-Berlin-400x225.jpg)























vielen Dank, dass Sie unseren Kommentar-Bereich nutzen.
Bitte verzichten Sie auf Unterstellungen, Schimpfworte, aggressive Formulierungen und Werbe-Links. Solche Kommentare werden wir nicht veröffentlichen. Dies umfasst ebenso abschweifende Kommentare, die keinen konkreten Bezug zum jeweiligen Artikel haben. Viele Kommentare waren bisher schon anregend und auf die Themen bezogen. Wir bitten Sie um eine Qualität, die den Artikeln entspricht, so haben wir alle etwas davon.
Da wir die Verantwortung für jeden veröffentlichten Kommentar tragen, geben wir Kommentare erst nach einer Prüfung frei. Je nach Aufkommen kann es deswegen zu zeitlichen Verzögerungen kommen.
Ihre Epoch Times - Redaktion