
Warum erkranken manche Menschen nicht an COVID-19?

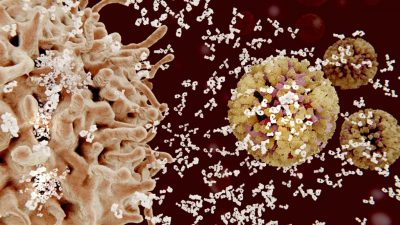
Das Immunsystem bildet ein komplexes Netzwerk, das ständig in Aktion ist. Millionen Immunzellen patrouillieren durch unseren Körper, überwachen Gewebe und reagieren auf Eindringlinge. Die Fähigkeit, uns vor Infektionen und Krankheiten zu schützen, basiert auf einem ausgeklügelten Kommunikationssystem und einer komplizierten Dynamik aktivierter Immunzellen. Dabei besitzen diese Zellen unterschiedliche und sehr spezifische Rezeptoren, die auf verschiedene Reize und Muster reagieren. Sie senden und empfangen Botenstoffe, die wiederum bestimmte Funktionen auslösen. Und sie zerlegen Eindringlinge, um ihre Bestandteile anderen Immunzellen zu präsentieren und eine koordinierte Abwehr zu ermöglichen.
Die genetische Ausstattung jedes Menschen, die auch die Aktivität der Immunzellen beeinflusst, ist höchst individuell. Dies zeigt sich deutlich in der Immunabwehr. Die Variation in den Genen kann erheblichen Einfluss darauf haben, wie unser Körper auf verschiedene Erreger, Viren oder Bakterien reagiert.
Eine neue Studie, die kürzlich in der angesehenen Fachzeitschrift „Nature“ veröffentlicht wurde, untersucht, wie individuell und komplex menschliche Immunsysteme auf SARS-CoV-2 reagieren und welche Faktoren für die unterschiedlichen Verläufe von Corona-Infektionen verantwortlich sind.
Kontrollierte COVID-19-Infektionen
Ein Team von Wissenschaftlern unter der Leitung von Sarah Teichmann von der University of Cambridge und Marko Nikolić vom University College London infizierte im Rahmen ihrer Untersuchung Freiwillige mit SARS-CoV-2. Die Teilnehmer durften zuvor weder eine COVID-19-Infektion durchgemacht noch eine Impfung erhalten haben.
Um die Dynamik der Immunabwehr gegen ein Virus genau zu verstehen, ist es entscheidend, den genauen Zeitpunkt der ersten Infektion zu kennen, erklären die Autoren der Studie. Der exakte Zeitpunkt der natürlichen Infektion ist jedoch bei Patienten oft nur schwer festzustellen oder gänzlich unbekannt.
Bei der Analyse der individuellen Immunreaktionen auf kontrollierte Infektionen stellten die Wissenschaftler deutliche Unterschiede in den Immunantworten der Teilnehmer fest. Von sechzehn infizierten Personen entwickelten lediglich sechs eine nachweisbare anhaltende COVID-19-Infektion, einschließlich positiver PCR-Tests und Symptome. Drei Personen zeigten innerhalb einer Woche mehrere sporadisch positive PCR-Tests, jedoch ohne Krankheitszeichen. Diese Fälle wurden von den Autoren als „vorübergehende Infektion“ eingestuft.
Natürliche Immunität gegen SARS-CoV-2 durch besonderes Gen
Interessanterweise blieben die übrigen sieben Teilnehmer PCR-negativ und symptomfrei, was darauf hindeutet, dass ihr Immunsystem in der Lage war, sowohl eine anhaltende als auch eine vorübergehende Infektion zu verhindern. Um herauszufinden, warum die Infektabwehr unterschiedlich erfolgreich war, isolierten die Forscher Immunzellen aus Abstrichen und Blutproben zu verschiedenen Zeitpunkten nach der Infektion. Dabei entdeckten sie signifikante Unterschiede in der Zusammensetzung und Aktivität bestimmter Immunzellen, die offenbar einen erheblichen Einfluss auf die Anfälligkeit für eine vorübergehende oder anhaltende symptomatische SARS-CoV-2-Infektion hatten.
Die Frage, warum einige Teilnehmer scheinbar immun gegen SARS-CoV-2 waren, wurde ebenfalls untersucht. Das Team analysierte die Immunzellen im Blut und im Nasen-Rachen-Raum einen Tag vor der Infektion. Es stellte sich heraus, dass bei den Teilnehmern, die später weder eine anhaltende noch eine vorübergehende Infektion entwickelten, ein bestimmtes Gen besonders aktiv war. Dieses Gen, HLA-DQA2, gehört zu den Humanen Leukozyten-Antigenen (HLA), die eine entscheidende Rolle bei der Antigenpräsentation und der Aktivierung von Immunzellen spielen.
Individualität als Schutz vor Krankheitserregern
HLA-Gene stehen seit Jahrzehnten im Mittelpunkt intensiver Forschung. Es wird vermutet, dass diese Gene im Verlauf einer Co-Evolution mit Mikroorganismen entstanden sind. Die hohe genetische Vielfalt der HLA-Gene spielt eine wesentliche Rolle bei der effektiven Abwehr gegen eine Vielzahl von Krankheitserregern.
Beim Menschen existiert eine große Bandbreite an HLA-Genen, die unterschiedliche Antigene präsentieren können. Diese genetische Variabilität innerhalb einer Population erhöht die allgemeine Widerstandsfähigkeit gegenüber Infektionen, da immer einige Individuen besonders effektiv auf bestimmte Erreger reagieren können.
Frühere Untersuchungen haben bereits gezeigt, dass bei Patienten mit schwerem COVID-19-Verlauf deutlich weniger HLA-DQA2 im Blut nachweisbar ist als bei Patienten mit mildem Verlauf. Die Autoren der aktuellen Studie schließen nun aus ihren neuen Beobachtungen, dass Immunzellen, die mehr HLA-DQA2 produzieren, besser vor SARS-CoV-2-Infektionen schützen können.
Die neue Veröffentlichung in „Nature“ verdeutlicht, wie komplex und individuell die Infektabwehr gegen Viren ist. Die detaillierte Beobachtung der Immunreaktionen und die neuen Einsichten zur unterschiedlichen Beteiligung von Immunzellen an der Abwehr könnten entscheidende Puzzlestücke für ein besseres Verständnis des Krankheitsverlaufs bei COVID-19 darstellen.
Diese Daten könnten auch dabei helfen, das Risiko für schwere COVID-19-Verläufe bei Menschen mit bestimmter genetischer Ausstattung genauer einzuschätzen. Die Identifizierung von Genen, die Schutz bieten, könnte dabei unterstützen, die Risikobewertung zu verfeinern.































vielen Dank, dass Sie unseren Kommentar-Bereich nutzen.
Bitte verzichten Sie auf Unterstellungen, Schimpfworte, aggressive Formulierungen und Werbe-Links. Solche Kommentare werden wir nicht veröffentlichen. Dies umfasst ebenso abschweifende Kommentare, die keinen konkreten Bezug zum jeweiligen Artikel haben. Viele Kommentare waren bisher schon anregend und auf die Themen bezogen. Wir bitten Sie um eine Qualität, die den Artikeln entspricht, so haben wir alle etwas davon.
Da wir die Verantwortung für jeden veröffentlichten Kommentar tragen, geben wir Kommentare erst nach einer Prüfung frei. Je nach Aufkommen kann es deswegen zu zeitlichen Verzögerungen kommen.
Ihre Epoch Times - Redaktion