
Der Beipackzettel: Corona-Schnelltests im Überblick – Anwendung nur bei COVID-Verdacht
Seit vergangener Woche sind die Corona-Schnelltests für jedermann im Handel erhältlich. Beim Bundesinstitut für Arzneimittel- und Medizinprodukte (BfArM) sind insgesamt (Stand 8. März) 221 sogenannte Antigentests auf SARS-CoV-2 gelistet.
Nach Mitteilung des Paul-Ehrlich-Instituts vom 5. März wurden 70 der Corona-Schnelltests als „dem derzeitigen Stand der Technik entsprechend“ bewertet, davon kommen 28 aus China, rund zehn aus Deutschland. Weitere Tests stammen aus Südkorea, den USA, der Schweiz und Frankreich.
In Deutschland gibt es derzeit (Stand 8. März) jedoch lediglich sieben Corona-Schnelltests, die für Laien geeignet sind. In ihrer Anwendung ähneln sie einem Schwangerschaftstest. Laut Bundesinstitut für Arzneimittel- und Medizinprodukte (BfArM) handelt es sich dabei um folgende Tests:
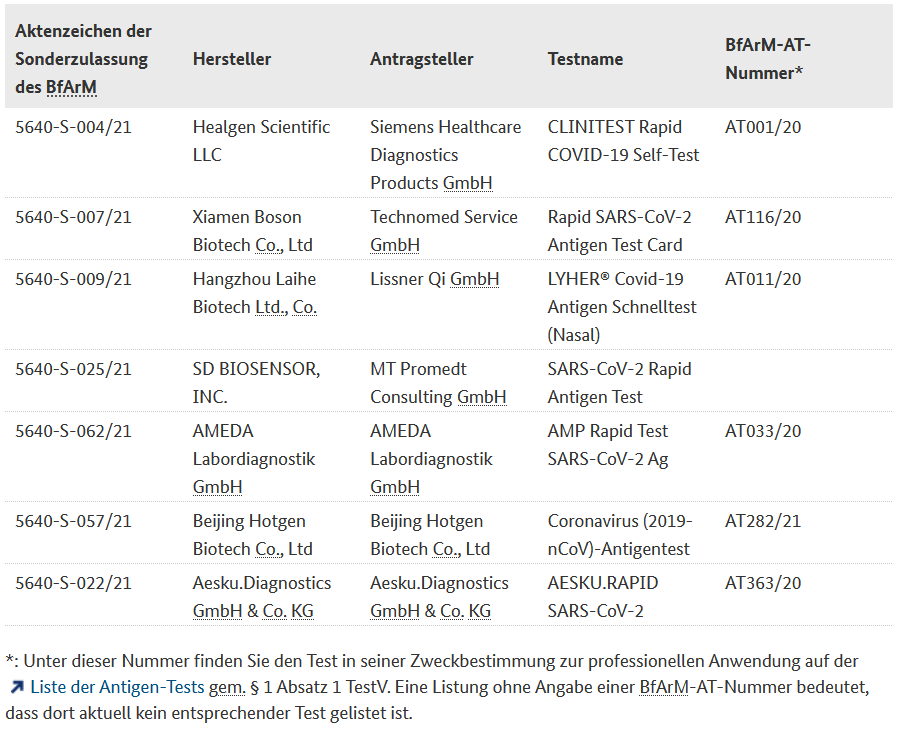
Übersicht der zugelassenen Laien-Schnelltests des BfArM. Foto: Screenshot BfArM
Test von Roche
Sechs dieser Tests sind ursprünglich zur professionellen Anwendung bestimmt gewesen und haben nun eine Sonderzulassung des BfArM erhalten, um auch von Laien angewandt zu werden. Der Test von SD BIOSENSOR aus dem Hause Roche bildet bislang die einzige Ausnahme. Er gilt ausschließlich als Selbsttest für Laien. In der „Gebrauchsanweisung für Patienten“ wird jedoch darauf verwiesen, dass der Test zum Nachweis von Antigenen des SARS-CoV-2-Virus bei Personen mit Verdacht auf COVID-19 diene.
Ein positives Ergebnis bedeute, dass man „sehr wahrscheinlich an COVID-19 erkrankt“ sei. Daher solle sich der Getestete umgehend an einen Arzt oder das örtliche Gesundheitsamt wenden und die örtlichen Richtlinien zur Selbstisolation einhalten. „Gegebenenfalls wird Ihr Arzt einen Bestätigungstest mittels PCR verordnen“, heißt es weiter.
Bei einem negativen Testergebnis hingegen sei eine COVID-19-Erkrankung unwahrscheinlich. Trotzdem sollten weiterhin alle Schutz- und Hygienemaßnahmen eingehalten werden. Gleichzeitig weist der Hersteller darauf hin: „Auch bei einem negativen Testergebnis kann eine Infektion vorliegen.“
Daher solle im Verdachtsfall, wenn Symptome weiterhin bestehen oder sich verschlimmern, der Test nach ein bis zwei Tagen wiederholt werden, „da das Coronavirus nicht in allen Phasen einer Infektion genau nachgewiesen werden kann.“
Test von Siemens
Die Gebrauchsanweisungen für die Tests sind unterschiedlich. So informiert US-Hersteller Siemens Healthcare Diagnostic Products GmbH in Houston bezüglich seines „CLINITEST Rapid COVID-19 Self-Test“ (des CLINITEST Rapid COVID-19 Antigen Tests) darüber, dass der Test „die schnelle Diagnose von SARS-CoV-2-Infektionen unterstützen“ soll.
Er soll von medizinischem Fachpersonal bis zu zehn Tagen nach Auftreten der Symptome angewendet werden. Die Schnelldiagnostik einer SARS-CoV-2-Infektion werde medizinischen Fachkräften helfen, „Patienten zu behandeln und die Erkrankung effizienter und effektiver zu kontrollieren“. Die Testprobe wird aus dem Nasen-Rachen-Raum oder dem unteren Nasenbereich entnommen.
„Positive Testergebnisse unterscheiden nicht zwischen SARS-CoV und SARS-CoV-2“, heißt es weiter. Der CLINITEST Rapid COVID-19 Antigen Test könne sowohl lebensfähiges als auch nicht lebensfähiges SARS-CoV-2 erkennen.
In einer weiteren veröffentlichten Beschreibung heißt es: „Produkt zur Eigenanwendung.“ Dafür wurde dieser Test in Deutschland befristet freigegeben. Begründet wird dies mit Paragraf 11 Medizinproduktegesetz und einer Anwendung „im Interesse des Gesundheitsschutzes“.
Statt einem Nasen-Rachen-Abstrich ist nun nur noch von einem Nasen-Abstrich die Rede. Bei Getesteten unter 15 Jahren soll der Test unter Aufsicht von Erwachsenen durchgeführt werden. Menschen über 70 wird geraten, sich unterstützen zu lassen. Wenn trotz negativem Testergebnis Symptome fortbestehen, wird empfohlen, eine „medizinische Fachkraft“ hinzuzuziehen.
Der Hersteller weist darauf hin:
Ein negatives Testergebnis schließt zu keiner Zeit das Vorhandensein von Coronaviren in der Probe aus, da diese unterhalb der Mindestnachweisgrenze des Tests vorhanden sein können.“
Ebenso könnten bei falscher Handhabung falsch negative Testergebnisse auftreten.
Weiter heißt es: „Wie bei allen in-vitro diagnostischen Tests sollte eine bestätigte Diagnose nur von einem Arzt gestellt werden, nachdem alle klinischen Befunde und Laborbefunde ausgewertet wurden.“ Gleichzeitig zeigt sich der Hersteller überzeugt: „Der Test kann feststellen, ob bei Ihnen eine COVID-19-Infektion vorliegt.“ Sofern das Ergebnis positiv ausfällt, müsse eine häusliche Isolierung durchgeführt und das Gesundheitsamt informiert werden.
Test BOSON SARS-CoV-2
Der in China hergestellte BOSON SARS-CoV-2 Antigen Schnelltest „Rapid SARS-CoV-2 Antigen Test Card“ wird in Deutschland von vier Herstellern unter unterschiedlichen Handelsnamen vertrieben; ein Unternehmen kommt aus Österreich.
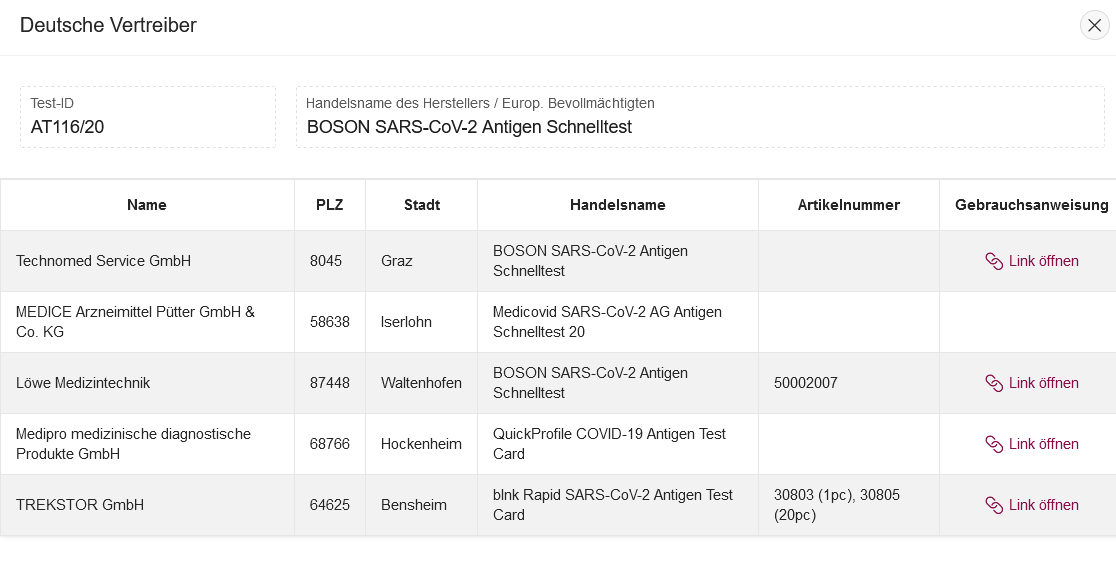
Auszug aus der Tabelle des BfArM, Test-ID AT116/20. Foto: Screenshot BfARM
Das Unternehmen Löwe Medizintechnik teilt gleich im ersten Absatz der Beschreibung mit: „Der SARS-CoV-2 Antigen Schnelltest dient nicht als Basis zur Diagnose oder dem Ausschluss einer Infektion mit SARS-CoV-2.“ Dieser Hinweis lässt sich auch auf den Beschreibungen der Medipro medizinische diagnostische Produkte GmbH und der TREKSTORE GmbH finden.
Unter „Vorsichtsmaßnahmen“ heißt es bei Löwe Medizintechnik weiter: „Das Produkt ist ausschließlich für den Gebrauch durch medizinisches Fachpersonal bestimmt und nicht für private.“ Wie bei allen diagnostischen Tests solle eine endgültige klinische Diagnose „nicht auf dem Ergebnis eines einzelnen Tests beruhen, sondern von der Ärztin beziehungsweise dem Arzt nach der Auswertung aller klinischen Ergebnisse und Laborbefunde gestellt werden.“ Der Test sei nicht für die Anwendung bei Patienten ohne Anzeichen und Symptome einer Atemwegsinfektion bewertet, und könne bei asymptomatischen Personen unterschiedlich sein.
Im vorletzten Satz der zweiseitigen Anleitung der Löwe Medizintechnik ist aufgeführt:
„Die Gültigkeit des SARS-CoV-2-Antigen-Schnelltests wurde für die Dentifizierung / Bestätigung von Gewebekulturisolaten nicht nachgewiesen und sollte in dieser Eigenschaft nicht verwendet werden.“
LYHER® Covid-19 Antigen Schnelltest
Ebenfalls aus China kommt der „Novel Coronavirus (COVID-19) Antigen Test Kit (Colloidal Gold), in Deutschland von der Lissner Qi GmbH als „LYHER® Covid-19 Antigen Schnelltest (Nasal)“ vertrieben. Das Produkt ist für Nasenrachen, Nasen- und Mundrachen-Sekretproben geeignet. Auch dieser Test darf laut Unternehmen „nur von geschultem Fachpersonal durchgeführt werden“.
Den Vorsichtsmaßnahmen ist die Warnung zu entnehmen: „Das Gerät enthält Material tierischen Ursprungs und ist als potenzielles biologisches Risiko zu behandeln.“ Bei diesem Testkit wurde der Kontrollbereich mit „Ziege-anti-Maus-igG-Antikörpern“ beschichtet.
Ein negatives Ergebnis schließt nicht die Möglichkeit einer COVID-19-Infektion aus“, so die Einschränkung des Tests.
Auch hier dürfe das Testergebnis nicht als alleinige Grundlage einer klinischen Diagnose und Behandlung herangezogen werden.
AMP Rapid Test SARS-CoV-2 Ag
In Österreich wurde ein weiterer Schnelltest von der AMEDA Labordiagnostik GmbH entwickelt. Dieser wird in Deutschland von der Dr. Lonsdorfer GmbH & Co. KG unter dem Handelsnamen „AMP Rapid Test SARS-CoV-2 Ag“ vertrieben. Der Test, für den Proben aus Nase, Nasen-Rachen-Raum und Rachen entnommen werden können, sei in der Lage, lebensfähige als auch nicht lebensfähige SARS-CoV-2 nachzuweisen. Vom Hersteller heißt es in der Gebrauchsanweisung:
„Ein negatives Testergebnis schließt das Vorhandensein von SARS-CoV-2-Antigenen in der Probe nicht aus, da die Antigenkonzentration unter der minimalen Nachweisgrenze liegen kann oder die Probe möglicherweise unsachgemäß entnommen oder transportiert wurde.“
ANTIGEN Laientest Antigentest (Kolloidales Gold)
Ein weiterer Schnelltest stammt aus Peking, in Deutschland wird er von der Dr. Grob Healthcare GmbH als „ANTIGEN Laientest, Coronavirus (2019-nCoV-)-Antigentest (Kolloidales Gold)“ vertrieben. Für die Probe reicht ein Nasenabstrich aus. Auch hier wird darauf hingewiesen, dass das Testergebnis nicht das „einzige Bestätigungskennzeichen für klinische Indikationen“ sei.
Ein negatives Testergebnis schließe die Möglichkeit einer Infektion nicht aus. Das Produkt diene „nur als Notfallreserve im Rahmen eines Lungenentzündungsausbruchs einer neuartigen Coronavirus-Infektion“. Es könne nicht als routinemäßiges Diagnostik-Reagenz für klinische Anwendung genutzt werden und sei nur für den professionellen Gebrauch geeignet.
AESKU.RAPID SARS-CoV-2
In Deutschland hergestellt ist der AESKU.RAPID SARS-CoV-2 der Aesku.Diagnostics GmbH & Co. KG aus Wendelsheim in Rheinland-Pfalz. Auch dieser ist laut Hersteller ursprünglich von medizinischem Fachpersonal durchzuführen. Als Proben dienen Nasenabstriche.
Negative Testergebnisse würden COVID-19 nicht vollkommen ausschließen, während bei einem positiven Testergebnis weiterhin eine klinische Anamnese notwendig sei, um den Infektionsstatus zu bestimmen.
Sondergenehmigung für Laientests
Wie das BfArM auf Nachfrage gegenüber Epoch Times mitteilte, ist mit einer Änderung der Medizinprodukte-Abgabeverordnung die Abgabe von Tests an Laien seit Anfang Februar 2021 grundsätzlich möglich geworden. Inzwischen liegen dem BfArM rund 100 Anträge auf Sonderzulassung von Laientests vor, erklärte Pressesprecherin Anja Kremzow.
Unabhängig von diesen Sonderzulassungen sei der Marktzugang für Laientests weiterhin über die CE-Kennzeichnung durch sogenannte „Benannte Stellen“ möglich. In diesen regulären Weg des Marktzugangs für Medizinprodukte sei die Behörde jedoch nicht eingebunden.
Die Prüfdauer von Sonderzulassungsverfahren hänge ganz wesentlich von der Qualität und Vollständigkeit der beim BfArM eingereichten Daten ab. Um solche Laientests schnellstmöglich verfügbar zu machen, führe das Institut alle Sonderzulassungsverfahren mit höchster Priorität im sogenannten „rolling review“ durch und unterstütze Hersteller bei der Antragstellung.
Dass die Anforderungen an die Verlässlichkeit der sogenannten Laientests sinken, müsse laut BfArM nicht befürchtet werden. Eine sichere Anwendung solle ebenso gewährleistet werden wie ein „wirksamer Beitrag zur Pandemiebekämpfung“, den die Schnelltests leisten könnten. Für eine Sonderzulassung müssen die Laientests daher bereits über eine CE-Kennzeichnung des Produktes für professionelle Anwender verfügen und positiv durch das Paul-Ehrlich-Institut evaluiert worden sein. Weiterer Schwerpunkt der BfArM-Prüfung sei ein Nachweis zur Gebrauchstauglichkeit der Tests.
Die Anforderungen im Sonderzulassungsverfahren benannte das BfArM wie folgt:
- Nachweis des Antrages für ein reguläres Konformitätsbewertungsverfahren bei einer europäischen benannten Stelle – sofern keine benannte Stelle den Antrag annimmt, eine Kopie der Ablehnung von mindestens zwei benannten Stellen, CE-Kennzeichnung des Produktes für professionelle Anwender. Positive Evaluierung des Produktes für professionelle Anwender durch das Paul-Ehrlich-Institut (PEI).
- Erfüllung der aktuellen Mindestkriterien des Paul-Ehrlich-Instituts (PEI), für die Eigenanwendung vorgesehene Gebrauchsanweisung in deutscher Sprache, Umverpackung des Produktes für die Eigenanwendung, Gebrauchstauglichkeitsstudie nach IEC 62366, Nachweis des Erfüllens der speziell für die Laienanwendung spezifizierten Grundlegenden Anforderungen aus Anhang I Nr. 7 der RL 98/79/EG, aktuelle Risikoanalyse.
Da der reguläre Marktzugang für Medizinprodukte über die CE-Kennzeichnung erfolgt, könne das BfArM keinen Überblick über alle in Deutschland auf dem Markt befindlichen Tests und auch keine Auskunft zum Vertrieb der jeweiligen Tests geben.
Zuverlässigkeit der Schnell- und Selbsttests in Frage gestellt
Während die bisher üblichen PCR-Tests genetisches Material des SARS-CoV-2 nachweisen sollen, geht es bei den Antigen-Tests darum, die zum Virus gehörenden Proteine zu erkennen. Im Gegensatz zum PCR-Test, der für das Robert Koch-Institut als „Goldstandard“ gilt, unter Ärzten und Wissenschaftlern aber umstritten ist, stuft Labormediziner Matthias Orth die Antigen-Tests als nicht so zuverlässig ein.
Für Dr. Michael J. Mina von der Harvard School of Public Health, ist jedoch auch der aktuelle PCR-Test „kein angemessener Goldstandard“.
In einem Kommentar in „The Lancet“ scheibt er: „Infizierte Personen sind [meist] 4-8 Tage lang ansteckend […], was die Gesundheitsbehörden dazu veranlasste, eine 10-tägige Isolationszeit zu empfehlen. Das kurze Zeitfenster der Übertragbarkeit steht im Gegensatz zu einem Median von 22-33 Tagen der PCR-Positivität (länger bei schweren Infektionen und etwas kürzer bei asymptomatischen Personen). Dies legt nahe, dass 50 bis 75 Prozent der Zeit, in der eine Person PCR-positiv ist, sie wahrscheinlich postinfektiös ist.“
Ob das Gleiche für Corona-Schnelltests zutrifft, ist bislang ungeklärt.
Unterschiedlicher Umgang mit Corona-Schnelltests und Selbsttests
Ein Corona-Schnelltest wird auch Antigentest oder POC-Test genannt, erklärte Tilla Steinbach, Pressesprecherin des Landkreises Mecklenburgische Seenplatte gegenüber Epoch Times. Schnelltests werden beispielsweise in Apotheken, Pflegeheimen und Arztpraxen angeboten.
Die Antigen-Schnelltests müssen von geschultem, medizinischem Personal durchgeführt werden. Wenn ein Schnelltest positiv ausfalle, dann werde dies namentlich an das zuständige Gesundheitsamt im Rahmen der Meldepflicht gemeldet. Anschließend werde normalerweise ein PCR-Test durchgeführt, um das Ergebnis des Schnelltests zu überprüfen, so die Pressesprecherin weiter.
Selbsttests hingegen seien zur Anwendung durch Privatpersonen bestimmt. Die Selbsttests hätten gegenüber den PCR-Tests eine höhere Fehlerrate. Daher müsse laut Bundesgesundheitsministerium nach jedem positiven Selbsttest immer ein PCR-Test zur Bestätigung gemacht werden. Eine Meldepflicht bestehe jedoch nicht.
Eine Meldepflicht für einen positiven #Selbsttest gibt es zurzeit nicht. Dennoch gilt:
1. Lassen Sie ein positives Ergebnis durch einen #PCR-Test bestätigen.
2. Begeben Sie sich zuhause in #Quarantäne, bis das PCR-Testergebnis vorliegt. pic.twitter.com/9xvESdhxDx
— BMG (@BMG_Bund) March 7, 2021
Mit Klick auf den folgenden Button stimmen Sie zu, dass der Inhalt von Twitter geladen wird.
Auf Nachfrage der Epoch Times teilte RKI-Pressesprecherin Marieke Degen mit:
Antigentests erfüllen, wenn keine PCR-Bestätigung durchgeführt worden ist, nicht die Referenzdefinition, sie werden also nicht in der RKI-Statistik veröffentlicht (siehe Falldefinitionen). Angaben über negative Antigentests werden nicht übermittelt.“
In Deutschland werden die Corona-Schnelltests für den Privatgebrauch inzwischen bei Aldi und Lidl angeboten, auch Rossmann, dm, Edeka und Rewe wollen den Verkauf in Kürze starten. Auch das Angebot von Netto und Penny soll um die Selbsttests erweitert werden. Aldi hatte bereits am 6. März mit dem Verkauf begonnen. Schnell waren die Packungen vergriffen. Ob jeder, der sich positiv testet, tatsächlich den Weg der Selbstisolation und einer PCR-Nachprüfung geht, bleibt zunächst seine persönliche Angelegenheit. Denn, wie bereits ausgeführt, gibt es aktuell keine Meldepflicht.
Hier geht es zu den Mindestkriterien des Paul-Ehrlich-Instituts für SARS-CoV-2- Antigentests, aktualisiert am 15. Januar 2021.
[Anm.d.Red.: Es kann sein, dass die Beipackzettel der frei verkäuflichen Corona-Schnelltests von den oben beschriebenen medizinischen Gebrauchsanleitungen abweichen.]
Unsere Buchempfehlung
Krankheiten wie COVID-19, Katastrophen und seltsame Naturereignisse machen den Menschen aufmerksam: etwas läuft schief. Es läuft tatsächlich etwas sehr schief. Die Gesellschaft folgt - verblendet vom "Gespenst des Kommunismus" - einem gefährlichen Weg.
Es ist der Kampf zwischen dem Guten und dem Bösen, zwischen dem Göttlichen und dem Teuflischen, die in jedem Menschen wohnen.
Dieses Buch schafft Klarheit über die verworrenen Geheimnisse der Gezeiten der Geschichte – die Masken und Formen, die das Böse anwendet, um unsere Welt zu manipulieren. Und: Es zeigt einen Ausweg. „Chinas Griff nach der Weltherrschaft“ wird im Kapitel 18 des Buches „Wie der Teufel die Welt beherrscht“ analysiert. Hier mehr zum Buch.
Jetzt bestellen - Das dreibändige Buch ist sofort erhältlich zum Sonderpreis von 50,50 Euro im Epoch Times Online Shop
Das dreibändige Buch „Wie der Teufel die Welt beherrscht“ untersucht auf insgesamt 1008 Seiten historische Trends und die Entwicklung von Jahrhunderten aus einer neuen Perspektive. Es analysiert, wie der Teufel unsere Welt in verschiedenen Masken und mit raffinierten Mitteln besetzt und manipuliert hat.
Gebundenes Buch: Alle 3 Bände für 50,50 Euro (kostenloser Versand innerhalb Deutschlands); Hörbuch und E-Book: 43,- Euro.
Weitere Bestellmöglichkeiten: Bei Amazon oder direkt beim Verlag der Epoch Times – Tel.: +49 (0)30 26395312, E-Mail: buecher@epochtimes.de



























vielen Dank, dass Sie unseren Kommentar-Bereich nutzen.
Bitte verzichten Sie auf Unterstellungen, Schimpfworte, aggressive Formulierungen und Werbe-Links. Solche Kommentare werden wir nicht veröffentlichen. Dies umfasst ebenso abschweifende Kommentare, die keinen konkreten Bezug zum jeweiligen Artikel haben. Viele Kommentare waren bisher schon anregend und auf die Themen bezogen. Wir bitten Sie um eine Qualität, die den Artikeln entspricht, so haben wir alle etwas davon.
Da wir die Verantwortung für jeden veröffentlichten Kommentar tragen, geben wir Kommentare erst nach einer Prüfung frei. Je nach Aufkommen kann es deswegen zu zeitlichen Verzögerungen kommen.
Ihre Epoch Times - Redaktion